Onkologische Forschung des Jean-Uhrmacher-Institutes
Unsere Arbeitsgruppe beschäftigt sich mit der Erforschung von Kopf-Hals-Tumoren. Dabei liegt unser Focus insbesondere bei durch Humane Papillomviren (HPV) verursachten Oropharynxtumoren. Wir analysieren Tumorproben mit modernen arraybasierten Techniken wie aCGH, mRNA- und miRNA-Arrays und verfügen über ein breites molekularbiologisches und immunhistochemisches Analysespektrum. Ziel unserer Arbeit ist es, im Rahmen individualisierter Behandlungsstrategien prognostisch und therapeutisch relevante Veränderungen zu identifizieren.
Karzinome im Kopf-Hals-Bereich (Head and Neck Squamous Cell Carcinoma, HNSCC) gehören weltweit zu den häufigsten Krebserkrankungen. Krankheitsauslösend sind häufig langjähriger Konsum von Tabak und Alkohol, sowie Infektionen mit Humanen Papillomviren (HPV) [1]. Insbesondere der Oropharynx ist von HPV-Infektionen betroffen (Oropharyngeal Squamous Cell Carcinoma, OPSCC). Mittlerweile kann von mehr als 50% HPV-indizierter OPSCC ausgegangen werden. Weltweit ist eine kontinuierliche Zunahme HPV-positiver OPSCC zu beobachten und zukünftig könnten diese sogar die Inzidenz von Karzinomen der Cervix uteri übertreffen [2]. Die meisten OPSCC Patienten werden in Deutschland operiert, oft zusätzlich kombiniert mit Radio(-Chemo)-Therapie.
Zitate:
- C. U. Hübbers and B. Akgül, “HPV and cancer of the oral cavity.,” Virulence, vol. 6, no. 3, pp. 244–248, 2015.
- A. K. Chaturvedi, E. A. Engels, R. M. Pfeiffer, B. Y. Hernandez, W. Xiao, E. Kim, B. Jiang, M. T. Goodman, M. Sibug-Saber, W. Cozen, L. Liu, C. F. Lynch, N. Wentzensen, R. C. Jordan, S. Altekruse, W. F. Anderson, P. S. Rosenberg, and M. L. Gillison, “Human Papillomavirus and Rising Oropharyngeal Cancer Incidence in the United States,” Journal of Clinical Oncology, vol. 29, no. 32, pp. 4294–4301, Nov. 2011.
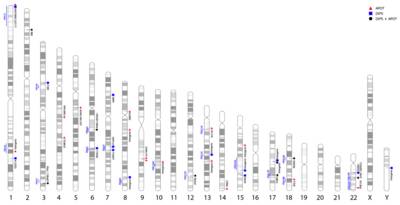
Die virale DNA kann sowohl als extrachromosomales Episom als auch in das Wirtsgenom integriert vorliegen. Die Integration der Virus-DNA in das Wirtsgenom ist nicht Teil des natürlichen viralen Lebenszyklus und könnte die maligne Transformation zur Tumorzelle fördern. Unterschiede in der Genexpression sind in Abhängigkeit vom Integrationsstatus der viralen DNA tatsächlich nachweisbar und beeinflussen möglicherweise den klinischen Verlauf und das Outcome von OPSCC-Patienten (Huebbers et al., eingereicht).
Die virale DNA liegt zunächst als eigenständiges, zirkuläres Molekül vor. Im Verlauf der malignen Progression kann diese DNA dann in das Wirtszellgenom integrieren, wobei Teile der viralen DNA verloren gehen, die Haupt-Onkogenen E6 und E7 allerdings erhalten bleiben. Das Gen für das virale E2 Protein wird dabei zerstört. E2 reguliert die Expression von E6 und E7, weswegen angenommen wird, dass die virale Integration mit E2-Verlust einen essentiellen Schritt in der Tumorprogression darstellt, da E6 und E7 nun unkontrolliert exprimiert werden.Wir konnten für OPSCC eine Integration der viraler DNA in das Wirtszellgenom bei 39% der Tumoren nachweisen und eine Präferenz der Integrationsereignisse für transkribierte Bereiche des Genoms der Wirtszellen zeigen. Allerdings hatte die virale Integration entgegen dem gängigen Modell keinen direkten Einfluss auf die Expression viraler Proteine (E2, E6, E7) und von einer viralen Integration betroffener humaner Genprodukte (z. B. TP63, HDAC2, FANCC). HPV-positive Tumorzellen regulieren die viralen Onkogene und von einer Integration betroffene eigene Gene auf einem eher konstantem denn signifikant verändertem Niveau (Olthoff, Huebbers et al., PLOS ONE 2014).
Viele Tumore weisen Besonderheiten im Glukosestoffwechsel auf (Warburg-Effekt). Bekannt ist, dass Mitochondrien von Kopf-Hals-Tumorzellen eine hohe Frequenz an Mutationen aufweisen. Daher haben wir zunächst Mutationen der mitochondrialen DNA (mtDNA) im Tumorgewebe, in Metastasen, Blut und im Speichel von Patienten mit Oropharynx-Tumoren untersucht. Zudem wurde die Glukoseaufnahme im Tumorgewebe vor Beginn der Therapie mittels 18FDG-PET quantifiziert. Immunhistochemisch wurde die Aktivität der mitochondrialen ATPase auf zellulärer Ebene quantifiziert. Wir konnten erstmals für Kopf-Hals-Tumoren zeigen, dass die Glukoseaufnahme direkt mit der Aktivität der mitochondrialen ATPase und letztlich mit der Malignität des Tumors korreliert. Hieraus ergeben sich potentielle therapeutische Ansätze über eine spezifische Inhibition der mitochondrialen Atmungskette (Huebbers et al., Oncotarget 2015). Weitergehende Untersuchungen zur Aufklärung der komplexen Tumorzellbiologie sind Bestandteil unserer aktuellen Projekte.
Während im HPV16-Genom insgesamt auffällig wenig Methylierungsstellen zu finden sind, können in der viralen Long Control Region LCR zwei Cluster identifiziert werden, die eine Bindung des viralen E2-Proteins regulieren. Die distalen E2-Bindungsstellen (E2BS) wirken sich dabei hyperaktivierend auf die Expression der viralen Onkogene E6 und E7 aus, während die proximalen E2BS eine Deaktivierung von E6 und E7 verhindern. Wir konnten insbesondere für die proximalen E2-Bindungsstellen deutlich unterschiedliche Methylierungsmuster erkennen. Eine Korrelation mit prognostischen Daten hat gezeigt, dass eine mittlere Methylierungsfrequenz (20-80% Methylierung) häufig mit einem intakten E2-Leseraster einher geht (d.h. nicht integrierte virale DNA). Bei hoher Methylierungshäufigkeit korreliert dies mit gemischtem Vorkommen von integrierten und episomalen viralen Kopien, bei der niedrigen Methylierungshäufigkeit mit einem unterbrochenem E2-Leseraster (integriertes Virus) (Reuschenbach, Huebbers et al., Cancer 2015). Somit könnte die Methylierungsanalyse ein guter Marker für die prognostisch relevante virale Integrationsanalyse sein.




